细胞起始材料
用于细胞和基因治疗的原代细胞
新鲜和低温保存的原代细胞用于细胞和基因疗法的发现和工艺开发,既可作为疗效和效力研究中的治疗靶点,也可作为安全性研究中的免疫测定,还可作为工艺开发、生产和培训的起始材料。
无论您处于哪个开发阶段:请以科学为导向设计您的实验,并与 BIOMEX 合作将其付诸实践!
了解 BIOMEX 如何帮助您将疗法从发现推向临床、缩短上市时间并降低产品线风险。
新鲜白细胞片
新鲜白细胞片是根据 IRB 批准的方案,从健康且同意的捐献者血液(白细胞抽吸术)中提取细胞浓缩过程的结果。新鲜白细胞片可用作分离特定免疫细胞类型的起始材料,以便在发现阶段低温保存和使用,或用作工艺开发的起始材料。白细胞浆中的白细胞浓度高于全血,单核细胞 (MNC) 的浓度高于水包衣(典型浓度为 20%单核细胞、50% T 细胞、10% B 细胞、10% 自然杀伤细胞、3% 粒细胞)。
从白细胞瘤中分离出单个细胞类型可以获得高细胞产量,并减少实验之间因供体不同而产生的差异。然而,考虑到供体的个体特征(如年龄、身高、性别、体重指数、吸烟习惯或特定的临床病史)可能会导致检测性能和细胞成分之间比例的变化,这一点非常重要。在研究中增加供体的变异性可以提高最新开发阶段的流程稳健性,甚至可以从异常值中获得重要的洞察力。如果您有兴趣在安全性研究中整合更多供体变异性,请查看我们的免疫原性-免疫毒性页面,或联系我们。
新鲜的 白细胞 在灌装时至少要达到 100 亿(整袋 Leukopak)或 50 亿(半袋 Leukopak)。然而,我们选择优先考虑交货速度和产品质量,而不是绝对的细胞数,如果总细胞数与标明的最低细胞数相比偏差>5%,下一订单的一袋产品将自动打折
新鲜的白细胞袋由 BIOMEX 在德国自己的血浆中心直接分离和运送,并可在分离后 24 小时内送达整个中欧地区。血浆分离后,您将收到一个跟踪链接,其中包含协议、分析证书和其他相关详细信息。分析证书上报告的参数包括人口统计学数据和供体信息、HLA 分型、全血细胞计数和供体水平的病原体检测。可根据要求增加其他检测项目。
如需了解个别供体规格的交货时间、召回特定供体的可能性或向中欧以外国家供货的情况,请联系我们的销售团队。
冷冻白细胞片
低温保存的白细胞片是根据 IRB 批准的方案,从健康且同意的捐献者血液(白细胞抽吸术)开始,经过细胞浓缩过程,然后再经过控制速率的低温保存步骤而得到的。冷冻保存的白细胞片可用作分离特定免疫细胞类型的起始材料,以便在发现阶段进一步冷冻保存和使用,或用作工艺开发的起始材料。在这方面,低温保存的白细胞片尤其适用于工艺开发,因为它能使实验计划与原材料的物流脱钩,让您随时可以开始实验,并在过程中节省重要的时间和资源。
白细胞分离中的白细胞浓度高于全血,单核细胞 (MNC) 的浓度高于水包衣(典型浓度为 20%单核细胞、50% T 细胞、10% B 细胞、10% 自然杀伤细胞、3% 粒细胞)。细胞存活率和不同细胞群的细胞数在新鲜和低温保存的白细胞片中相似,并在分析证书上报告。
分析证书上报告的参数包括人口统计学数据和供体信息、HLA 分型、全血细胞计数和供体水平的病原体检测。新产品可根据要求增加其他检测项目。
如需咨询个别捐献者规格的交货周期、召回特定捐献者的可能性或向中欧以外国家供货的情况,请与我们联系。
外周血单核细胞
PBMC(外周血单核细胞)是外周血白细胞的一部分,包括 T 和 B 淋巴细胞、NK 细胞、单核细胞和树突状细胞。外周血单核细胞通常被用作分离特定细胞亚群的起始材料,以用于不同的检测。
白细胞介导细胞(PBMC)是通过密度梯度分离从白细胞瘤中制备的,并在进行细胞计数后低温保存。为了考虑冷冻保存过程中可能出现的细胞损失,并保证达到规格中规定的最低存活细胞数,会对 PBMC 进行过量填充。冷冻的 PBMC 随后解冻,以进行质量控制,并确认其存活率和细胞数。BIOMEX 从自己的血浆中心分离出的白细胞中分离出 PBMC,并能保证在提取后 2 小时内进行冷冻保存,从而可大批量提供高质量、未受刺激的 PBMC,使多个实验具有最佳的一致性。
BIOMEX 的 PBMCs 计划
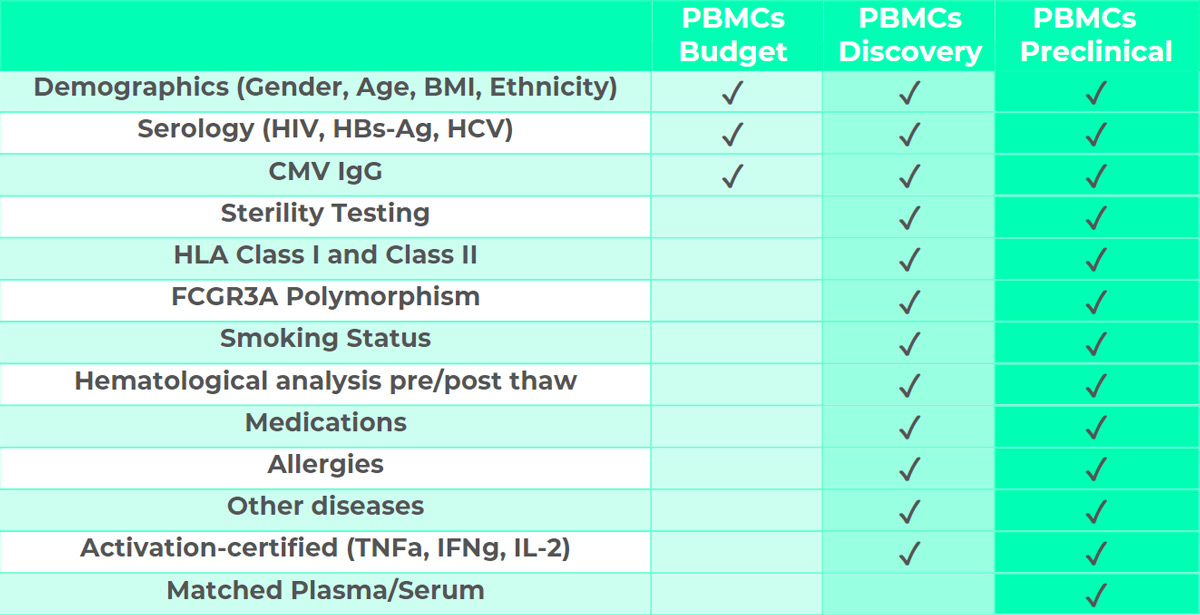
该计划专为基础研究设计,适用于初步研究或不需要高级供体相关信息的检测。PBMCs 预算细胞将进行血清学检测。如以下计划所示,只需支付少量费用,即可提供其他可选信息和检测。
该计划专为药物发现方法(包括靶点验证、先导物鉴定和优化)中使用的检测而设计。它提供完整的供体信息,包括人口统计学、血清学、HLA I 类和 II 类特征、FCGR3A 多态性、吸烟状况、解冻前和解冻后血液学分析、药物、过敏和其他疾病。白细胞介导细胞(PBMCs)–发现时进行无菌和细胞活化测试。
该计划用于临床前试验中使用的检测方法,包括免疫原性、免疫毒性、机理毒理学和研究毒理学。提供完整的供体信息,包括人口统计学、血清学、HLA I 类和 II 类特征、FCGR3A 多态性、吸烟状况、解冻前和解冻后血液学分析、药物、过敏和其他疾病。对发现的 PBMC 进行无菌和细胞活化测试。此外,还可提供来自同一患者的匹配血浆或血清(1 毫升低温保存等分样品)。
我们提供的细胞和基因疗法安全测试
细胞和基因疗法的安全性测试是临床前和临床开发过程中最重要的步骤之一。虽然包括 T 细胞受体工程 T 细胞 (TCR-T)、嵌合抗原受体 T 细胞 (CAR-T) 和肿瘤浸润淋巴细胞 (TIL) 在内的领养细胞疗法 (ACT) 被证明对癌症治疗非常有效,但它们也与轻微到危及生命的靶上毒性、脱靶毒性和免疫激活导致的毒性(如细胞因子释放综合征 (CRS))有关。同样,基因疗法也被报道与靶上和靶下毒性有关。此外,特别是腺相关病毒(AAV),为克服针对帽侧蛋白的抗体产生的基线,必须使用高剂量的病毒载体,这导致了严重的不良事件,如肝毒性和背根神经节毒性。
我们提供的细胞和基因疗法安全性测试包括用于免疫原性和免疫毒性测试的 PBMCs 面板,可使用或不使用匹配的血浆和血清。如果您希望节省时间和资源,我们的专家服务团队将与您合作,加速您的产品线进展。如需了解更多信息,请联系我们。
免疫原性和免疫毒性检测板
BIOMEX 的免疫原性和免疫毒性试剂盒设计用于支持临床前和临床阶段大分子、细胞疗法和基因疗法的内部安全性测试。试剂盒的配置适合再现白种人中最常见的 HLA I 类或 II 类等位基因的全部范围,适用于首次筛选试验。如果需要,我们还可根据客户要求组装用于特定等位基因检测的试剂盒。
免疫原性和免疫毒性试剂盒各 100 瓶,相当于 10 瓶 à 20 百万存活的低温保存 PBMCs/瓶/供体,供 10 位供体使用。对冷冻保存的 PBMCs 进行无菌、血清学和细胞活化测试,并预先进行 T 细胞增殖试验和 DC:T 细胞刺激试验。有关人口统计学、既往临床病史和解冻前后血液学分析的数据可应要求提供。
可提供以下检测版:
该检测板包含 10 个不同的供体,以涵盖白种人中最常见的 HLA I 类等位基因,通常也包含一些不常见的等位基因。ImmunoSafe™-HLA1 检测板为现货供应,可在次日发货。如果面板没有现货,交货期可能长达 3 周。如需咨询特定试剂盒的交货时间,请联系我们的销售团队。
该试剂盒包含 10 个不同的供体,以涵盖白种人中最常见的 HLA II 类等位基因,通常还包含一些不常见的等位基因。ImmunoSafe™-HLA2 血小板是现成产品,可在次日发货。如果面板没有现货,交货期可能长达 3 周。如需咨询特定试剂盒的交货时间,请联系我们的销售团队。
进一步了解我们的免疫原性和免疫毒性产品
匹配血浆和血清
可应要求提供配对血浆和血清,这些血浆和血清来自 ImmunoSafe™ 检测板中的供体,每份 1 毫升。对于定制试剂盒和新产品,前置时间可能长达 3 周。如需咨询特定试剂盒组成或不同等分试剂盒格式的交货时间,请联系我们。