免疫原性-免疫毒性
免疫原性和免疫毒性
免疫原性和免疫毒性是开发新的生物治疗药物、疫苗、细胞和基因疗法时需要考虑的潜在挑战,因此也是监管机构和科学界密切研究和讨论的领域。
免疫原性是指一种物质激发免疫反应的能力;免疫毒性是指一种物质因免疫系统功能紊乱而导致免疫系统或其他系统不良反应的能力。
免疫原性和免疫毒性在新型蛋白质疗法开发中的作用是什么?
对新型蛋白质疗法的免疫原性和免疫毒性风险进行评估是保证其安全性和有效性的关键,但这一工作也面临着一些挑战,包括不同人群之间免疫原性反应的差异、疫苗免疫原性随年龄的变化以及动物模型普遍不适合预测人体免疫反应等。
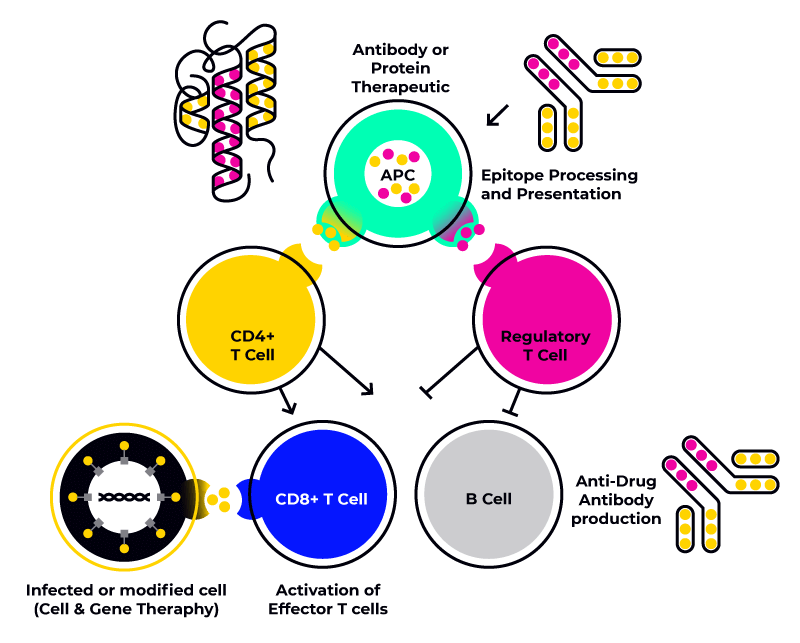
免疫毒性通常是任何治疗方法都不希望产生的效果,而免疫原性在新型蛋白质疗法中可能是期望的(想要的)效果,也可能是不期望的(不想要的)效果:
- 需要的免疫原性是疫苗疗效的一个核心方面,因为注射想要的抗原会激发针对抗原的免疫反应,从而产生针对活性病原体的保护作用。
- 不需要的免疫原性 是针对蛋白质疗法的不良免疫反应,通常会产生抗药抗体 (ADA),具有灭活或中和治疗剂的特性。
由于免疫原性的潜在不良影响,监管机构希望非疫苗生物疗法的开发商在临床开发阶段采用有效的免疫原性检测方法来检测和描述 ADA 形成的风险。在临床前免疫原性和免疫毒性评估期间,对新型蛋白质疗法的先天性和适应性免疫反应进行早期鉴定有助于降低开发管道的风险,并有助于深入了解其作用机制,或为临床开发阶段的患者细分提供线索。
免疫原性的机制是什么?
免疫原性机制可能涉及先天性免疫系统细胞(如单核细胞、巨噬细胞、NK 细胞、肥大细胞和中性粒细胞)和适应性免疫系统细胞(如巨噬细胞、树突状细胞、T 绒毛细胞、T 细胞毒性细胞、T 调节细胞和 B 细胞)。个体的 HLA 特征是导致免疫反应的一个重要因素,因此有必要研究来自具有目标人群代表性 HLA 特征的供体的细胞,以便准确地建立免疫原性检测。
生物治疗中的免疫原性
正是这第二种由 HLA II 类介导的机制导致了抗药抗体(ADA)的形成,从而降低了生物治疗药物的疗效,并引发了其他不良反应,包括超敏反应和治疗产品清除率升高。
由于 TCR 可识别 HLA 表位复合体,因此可以理解为什么特定的 HLA 等位基因被认为在多发性硬化症和类风湿性关节炎患者 ADA 的形成中起作用。因此,用目标人群中最常见的 HLA II 类等位基因或单倍型(由单亲遗传而来的一组等位基因)的免疫细胞(如 PBMC)代表性样本来筛选生物治疗剂非常重要。
由于 TCR 可识别 HLA 表位复合体,因此可以理解为什么特定的 HLA 等位基因被认为在多发性硬化症和类风湿性关节炎患者的 ADA 发病中起作用。因此,使用目标人群中最常见的 HLA II 类等位基因或单倍型(由单亲遗传而来的一组等位基因)的免疫细胞(如 PBMC)代表性样本来筛选生物治疗剂非常重要。
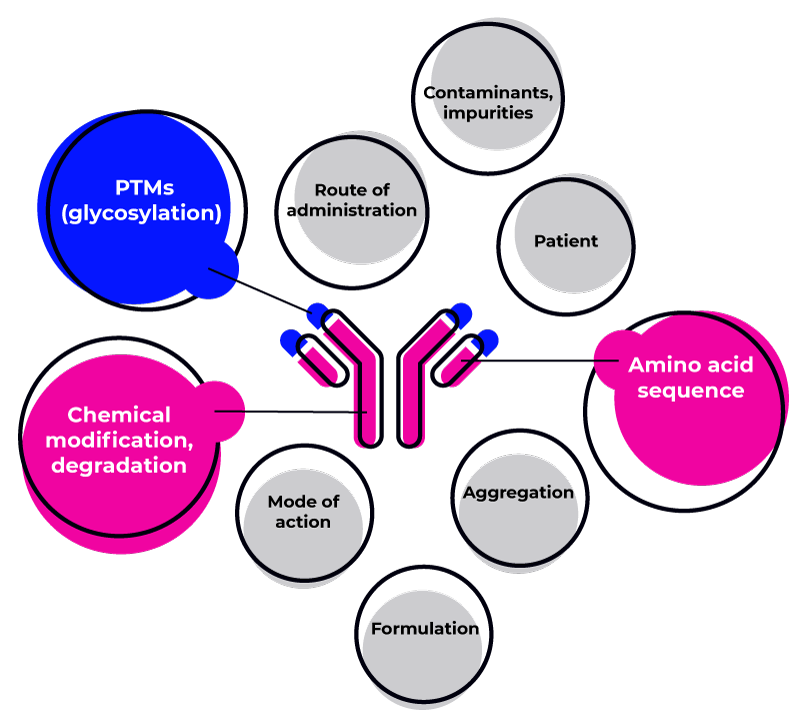
导致免疫原性的常见原因包括
-
患者的 HLA 等位基因
-
生物治疗药物的氨基酸结构
-
生物治疗药物可能出现的聚集现象
-
化学修饰或降解
-
给药途径
-
患者以前可能患过的疾病
-
杂质和污染
-
剂型和剂量
-
作用模式(如细胞内或细胞外靶点)
-
翻译后修饰 (PTM),如糖基化和 PEG-ilation
-
是否存在动物来源成分
-
生物治疗结构中是否存在动物源序列
评估生物治疗产品的免疫原性可以在临床前开发阶段进行。首先通过计算机模拟分析生物治疗产品中的表位,然后在最常见的HLA II类分子覆盖的免疫细胞上进行基于细胞的筛选,接着进行体外免疫原性试验,预测抗体结合和中和反应。在临床开发过程中,可以通过在患者血液样本中使用验证过的检测方法确认抗药性抗体(ADAs)
细胞和基因疗法及疫苗的免疫原性
HLA II 类介导的适应性免疫反应在针对生物治疗药物(不需要的免疫原性)和疫苗(想要的免疫原性)的免疫原性发展中发挥着重要作用,而 HLA I 类介导的免疫反应则在细胞疗法、基因疗法和疫苗的发展中发挥着重要作用。
细胞疗法是一种将细胞扩增并重新应用于受损组织的疗法。对于异基因细胞疗法,重要的是要考虑到如果供体的任何内源性蛋白质出现相关的多态性或表达不同的 HLA 等位基因,新的表位就会出现在 HLA I 类上,细胞就会被 NK 细胞或 CD8+ T 细胞毒性细胞清除。
基因疗法是在体内或体外对细胞进行基因改造的应用。与 ATMP 类似,对自体细胞或异源细胞的基因操作会导致引入新的序列和/或引入新的表位,新形成的表位将由 HLA I 类呈现,并有可能被 NK 细胞或 CD8+ T 细胞毒性细胞消除。
虽然对疫苗的反应在很大程度上依赖于通过 HLA II 类产生中和抗体的适应性免疫反应,但在病毒和其他细胞内病原体的情况下,CD8+ T 细胞毒性细胞的活化负责消灭受感染的细胞,从而阻止感染。由于 mRNA 疫苗的效力取决于受种者细胞中病原体衍生抗原的表达,因此监测 HLA I 类介导的免疫反应的激活情况至关重要,这样才能确保对病原体提供足够的保护,同时避免因 CD8+ T 细胞对疫苗抗原表达细胞产生毒性反应而在注射部位产生毒性。
因此,通过针对目标人群中最常见的 HLA I 类表达的免疫细胞进行测试来评估细胞和基因疗法及疫苗的免疫原性非常重要。
免疫原性测试使用哪些检测方法?
生物治疗药物、生物仿制药、细胞和基因疗法以及疫苗的开发需要对药物物质和药物产品的免疫原性风险进行广泛的分析。免疫原性风险评估基于多种检测方法,可帮助您了解治疗方法中免疫原性的发生和原因,并优化正确的策略。
临床前免疫原性评估的常用方法包括
-
表位分析
-
体外HLA I 类和 II 类结合试验
-
基于细胞的免疫原性试验,包括 T 细胞增殖试验、DC:T 细胞刺激和增殖试验以及 compley 模型中的 2D-3D 迁移和活化试验
-
使用人源化小鼠模型进行体内免疫原性评估
-
利用血浆或全血进行体内外检测,以检测 ADA
免疫毒性的机理是什么?
免疫毒性是指某种物质能够损害体液或细胞免疫反应,从而导致免疫抑制或造成不必要的组织损伤(如超敏反应、自身免疫或慢性炎症)。免疫毒性可分为靶上免疫毒性和非靶上免疫毒性。
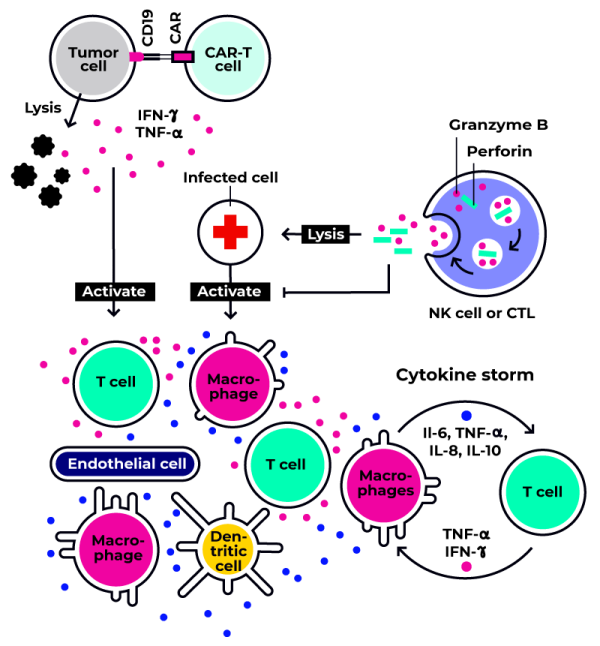
众所周知,免疫调节疗法以及基于免疫的 ATMP(如 CAR-T 细胞疗法)可能会因靶内和靶外的细胞损伤而诱发 CRS。因此,必须监测免疫毒性效应的可能发生情况,以便在早期开发过程中实施适当的策略。
靶向免疫毒性通常由免疫调节单克隆抗体(mAb)引起,可能是由于单克隆抗体与目标抗原或目标细胞/介质结合后导致其活性过度或持续增强。 这可能导致对具有多种免疫功能(包括没有治疗效益的功能)的目标进行调节,从而引发不良事件。
非靶向免疫毒性通常是由单克隆抗体(mAb)引起的,这些抗体靶向由非免疫细胞或其他非预期治疗靶点的细胞上呈现的表位或表达的靶点
细胞因子释放综合征(CRS)是免疫毒性最严重的后果之一,可能造成致命影响。在 CRS 中,细胞因子风暴是免疫系统针对病原体或外来物质正常激活的结果。在这一反应过程中,活化的巨噬细胞和树突状细胞会释放细胞因子,以招募和激活淋巴细胞并启动炎症过程。成功消灭靶细胞/受感染细胞后,炎症信号会进一步释放,并诱发淋巴细胞损伤。受损的淋巴细胞会进一步释放炎症细胞因子,增加免疫反应的强度,以至于炎症反应开始破坏健康组织,导致重要的功能性损害。
免疫毒性测试使用哪些检测方法?
免疫毒性是先导药物选择和进一步优化过程中的主要考虑因素之一,早期评估靶上和靶下毒性对于降低开发过程的风险至关重要。为了研究治疗策略的免疫毒性,了解其作用机制以及临床上可接受的患者风险/收益比非常重要。
评估免疫毒性的常用方法包括
-
计算机模拟表位分析
-
使用非靶组织的原代细胞进行基于细胞的脱靶毒性评估
-
基于细胞的 CRS 靶点毒性评估
-
体内研究(取决于药理学)
-
利用血浆或全血进行体内外检测,以检测 ADAs
免疫原性和免疫毒性检测板
BIOMEX 的免疫原性和免疫毒性试剂盒设计用于支持临床前和临床阶段大分子、细胞疗法和基因疗法的内部安全性测试。试剂盒的配置适合再现白种人中最常见的 HLA I 类或 II 类等位基因的全部范围,适用于首次筛选试验。如果需要,我们还可根据客户要求组装用于特定等位基因检测的试剂盒。
免疫原性和免疫毒性试剂盒各 100 瓶,相当于 10 瓶 à 20 百万存活的低温保存 PBMCs/瓶/供体,供 10 位供体使用。对冷冻保存的 PBMCs 进行无菌、血清学和细胞活化测试,并预先进行 T 细胞增殖试验和 DC:T 细胞刺激试验。有关人口统计学、既往临床病史和解冻前后血液学分析的数据可应要求提供。
可提供以下检测盘:
该检测盘包含 10 个不同的供体,以涵盖白种人中最常见的 HLA I 类等位基因,通常也包含一些不常见的等位基因。ImmunoSafe™-HLA1 检测板为现货供应,可在次日发货。如果面板没有现货,交货期可能长达 3 周。
该检测盘包含 10 个不同的供体,以涵盖白种人中最常见的 HLA II 类等位基因,通常还包含一些不常见的等位基因。ImmunoSafe™-HLA2 检测板为现货供应,可在次日发货。如果面板没有现货,交货时间可能长达 3 周。
如需咨询特定血清盘组合的交货时间,请联系我们。
匹配血浆和血清
可应要求提供配对血浆和血清,这些血浆和血清来自 ImmunoSafe™ 检测板中的供体,每份 1 毫升。对于定制试剂盒和新产品,前置时间可能长达 3 周。如需咨询特定试剂盒组成或不同等分试剂盒格式的交付周期。
免疫原性和免疫毒性服务
我们的免疫原性和免疫毒性服务旨在为您提供候选疗法风险概况的全面信息,使您能够进一步完善、人源化或工程化您的生物疗法,并评估其效力和疗效。
我们的策略包括进行硅学 和体外试验,以确定免疫原表位、研究免疫细胞的相互作用并确定合适的候选药物。
BIOMEX 已开发出一系列体外检测方法,包括
-
T 细胞活化和增殖
-
先天性免疫细胞活化和增殖
-
DC:T 细胞刺激试验
-
细胞因子风暴检测
如果您有兴趣开发新的检测方法或研究特定的作用机制,我们的服务团队将与您合作开发最佳解决方案。
欲了解更多有关如何降低疗法开发风险的信息: